Прогнозы не радуют: микроорганизмы могут распоясаться. После пандемии устойчивых к антибиотикам бактерий может стать в 3–4 раза больше. Сегодня эта проблема волнует медицинское сообщество не меньше, чем сам коронавирус. Всплеск резистентности равен отсутствию эффективных лекарств, которые могли бы справиться с суперинфекциями. Ученые всего мира активно изучают глобальную угрозу и продумывают пути решения. Наши исследователи не остаются в стороне. Корреспондент «Р» заглянула в лабораторию кафедры эпидемиологии и микробиологии БелМАПО, где стали изучать поведение бактерий на фоне коронавирусной инфекции.
 На разработку и производство принципиально нового противомикробного препарата необходимо 7—8 лет.
На разработку и производство принципиально нового противомикробного препарата необходимо 7—8 лет.Найти управу
Применение антибиотиков во время пандемии достигло серьезных масштабов во всем мире. На разработку и производство принципиально нового противомикробного препарата необходимо 7–8 лет. То есть каждые 7–8 лет на рынок выходит свежий продукт, а не аналоги. А бактерии, чтобы выработать устойчивый к антибиотику штамм, надо 4–5 лет. По прогнозам ученых, если человечество не начнет борьбу с устойчивостью микроорганизмов к антибиотикам, то к 2050 году мировая экономика потеряет 100 трлн долларов, а супербактерии тем временем совсем потеряют страх к имеющимся лекарствам. Люди смогут делать самые высокотехнологичные операции, но умирать от разбушевавшихся бактерий.— Зная всеобщую обеспокоенность, мы решили инициировать исследование: стали анализировать динамику частоты устойчивости выделенных микроорганизмов по отношению к антибактериальным препаратам на современном этапе, — доцент кафедры эпидемиологии и микробиологии БелМАПО Оксана Тонко соглашается устроить экскурсию по лаборатории. — На анализ попадают бактерии, которые выделяли у пациентов с коронавирусом и без него. COVID-19 — это вирус. Но никто не отменял других возбудителей, которые могут ухудшить течение болезни. Когда человек находится в реанимации, на искусственной вентиляции легких, риски инфекционного осложнения очень велики. Бактерии попадают из кишечника в легкие, лимфатическую систему, кровь. И если микроорганизм мутирует и приобретет суперспособность, читайте, устойчивость к антибиотикам, к дезинфектантам, антисептикам, то получает карт-бланш для распространения. Кстати, это еще один фактор, почему так важно вакцинироваться от COVID-19. Ведь привитые крайне редко оказываются в отделении интенсивной терапии и реанимации. Вне стационара бактерии не являются для нас чрезмерно опасными. Но если человек находится в тяжелом состоянии, на ИВЛ, его организм ослаблен, может присоединиться дополнительно бактериальная инфекция, которая в случае высокой устойчивости к антибиотикам крайне плохо поддается лечению.
Лаборатория кафедры сотрудничает с Минским городским центром гигиены и эпидемиологии и детской инфекционной клинической больницей, где для нее отбирают самые уникальные экземпляры бактерий — с множественной лекарственной устойчивостью. Можно сказать, самые опасные, на которые медикам еще попробуй найти управу.
«Кулинарный» процесс
— Лаборант Галина Борисенко сегодня на кухне, — так она шутит сама про себя.
Этот этап работы действительно можно сравнить с кулинарным процессом. Чтобы вырастить бактерию для дальнейших исследований, надо подготовить ей питательную среду.
Галина Борисенко показывает полку с множеством баночек. В каждой — уникальный состав, подходящий для бактерий разного вида. Основу составляют агар-агар, желатин, а потом уже идут добавки — вытяжки мяса, рыбы.
— При использовании классического микробиологического метода питательные среды варим на плите в средоварной, — Галина Николаевна засучивает рукава.
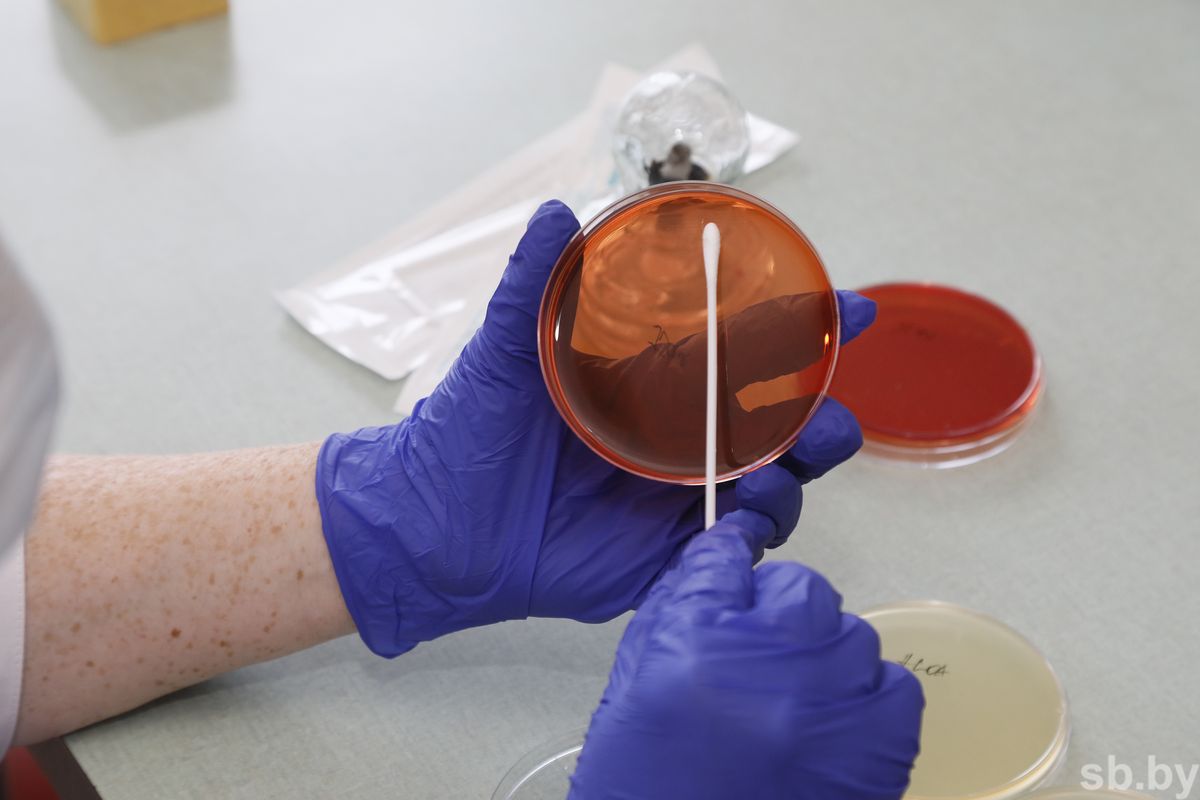 Чтобы вырастить бактерию для дальнейших исследований, надо подготовить ей питательную среду.
Чтобы вырастить бактерию для дальнейших исследований, надо подготовить ей питательную среду.
Сухая питательная среда смешивается с дистиллированной водой, доводится до кипения, определяется РН. Далее полученную субстанцию разливают по флаконам и отправляют в автоклав для стерилизации, где она под давлением подвергается воздействию температуры свыше 120 градусов. Это необходимо для обеспечения полной стерильности, чтобы не присоединилась другая микрофлора. Полученную питательную среду заливают в чашки Петри (они напоминают прозрачные контейнеры), а затем на них выращивают бактерии.
Оксана Тонко в напряжении склонилась над рабочим столом в лаборатории:
— Сейчас добавляю на питательный агар чистую культуру клебсиеллы пневмонии. Через сутки она размножится до нескольких миллиардов бактерий, и можно будет с ней проводить различные эксперименты, например смотреть, как она будет реагировать на отдельные антибиотики и их комбинации. Клебсиелла относится к супермикробам — часто устойчива к антибиотикам, которые обычно используются для лечения бактериальных инфекций. Страшный сон любого врача — получить антибиотикограмму, в которой напротив каждого антибиотика будет стоять буква R (resistant, устойчивый). Увы, такие эпизоды уже бывали. В Беларуси есть случаи выделения микробов с приобретенной устойчивостью ко всем известным группам препаратов. Проблема для пациента, для лечащего врача. Во время первой волны коронавируса медики всего мира не знали, как бороться с новой инфекцией. Было много необоснованных назначений антибиотиков, особенно в условиях амбулаторной практики. Устойчивые микроорганизмы получили преимущества для распространения.
Группа последней надежды
Чем чаще мы используем препарат, тем бактерии становятся устойчивее к нему. Поэтому в ежедневной практике запрещены резервные антибиотики. Чтобы назначить такое лекарство, собираются целые консилиумы врачей. Не потому, что такие препараты опасные. Наоборот, очень эффективные. Можно сказать, супергерои в борьбе с опасными бактериями. Но при постоянном использовании они потеряют свои качества. Поэтому группу резерва рассматривают как лекарственные средства последней надежды и использовать их необходимо только в самых тяжелых случаях.В лаборатории сейчас проходят сравнительные исследования частоты распространения устойчивых типов бактерий у госпитализированных пациентов до COVID-19 и во время пандемии. Сегодня уже можем сказать, что число множественно-устойчивых типов ацинетобактера и клебсиеллы (бактерии) в 2020 году по сравнению с 2019-м увеличилось для некоторых групп антибиотиков почти в два раза, достигая у пациентов с коронавирусной инфекцией 25 процентов. Факторы, которые могут повлиять на уровни устойчивости к противомикробным препаратам во время пандемии COVID-19, сегодня активно исследуются. Перед учеными и фармакологическими компаниями стоит задача разрабатывать свежие антимикробные препараты. Хотя создать что-то совершенно новое нелегко.
— Как выход — раннее распознавание проблемы и поиск путей преодоления устойчивости бактерий, — Оксана Тонко делает последовательные разведения антибиотика в пробирках, чтобы исследовать их минимальные концентрации, подавляющие рост бактерий. — Сейчас, например, подбираем комбинации антибиотиков, которые смогут преодолеть барьер устойчивости, выстроенный бактериями.
С другой стороны, каждый из нас может сам помочь решению проблемы. Нельзя самостоятельно принимать антибиотики, менять дозировку, способ и длительность курса. Досрочное прерывание курса терапии приводит к тому, что микробы не только выживают, но, образно говоря, становятся наглее и агрессивнее. Если доктор видит, что антибиотик не действует, его меняют на препарат из другой группы. Не стоит часто использовать одно и то же средство, даже если в прошлый раз оно быстро помогло выздороветь. Есть большая вероятность, что в организме может сохраняться устойчивый к нему штамм микроорганизма. И главное, помним об иммунитете. Лишь крепкому иммунитету по силам победить инфекцию без горсти лекарств.
azanovich@sb.by