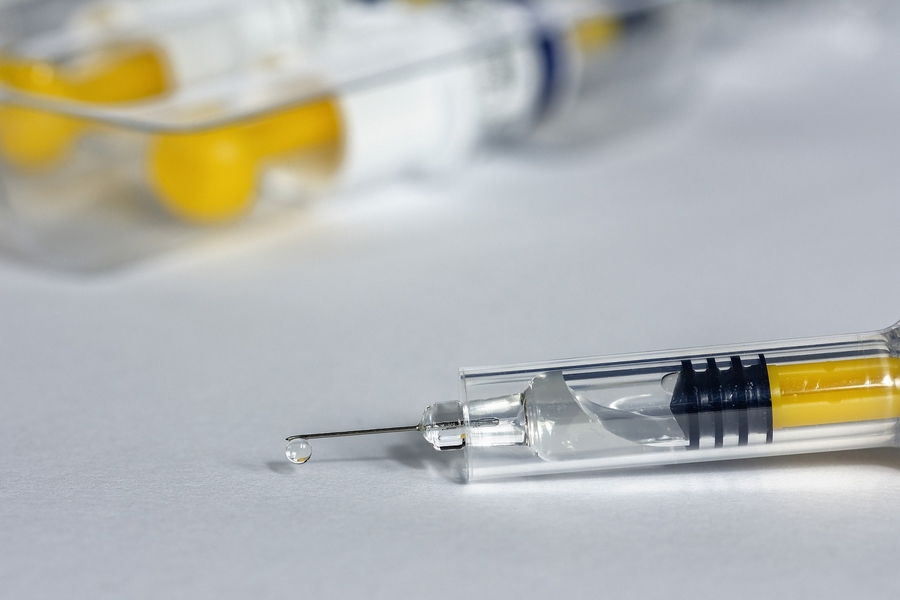
Вопрос, который сегодня волнует миллиарды людей: кто и когда изобретет вакцину от COVID-19? Среди стран, входящих в коалицию по разработке этого медицинского препарата, началась настоящая «гонка вооружений». США планируют разработать и начать массовый выпуск прививки уже в ближайшее время, Китай и вовсе обещает сделать ее бесплатной для всех желающих. Насколько эти заявления близки к реальности? Что происходит в ведущих лабораториях мира? И при каких условиях наша страна может войти в пул производителей вакцин?

Успеть за семь месяцев
Коварство нового вируса заключается в том, что его клетки постоянно видоизменяются, что значительно затрудняет разработку вакцины. По словам главного внештатного инфекциониста Минздрава, заведующего кафедрой инфекционных болезней БГМУ, профессора Игоря Карпова, происходящие с вирусом мутации объясняются его высокой приспосабливаемостью: он имеет длинную линейную РНК, которая способна подстраиваться под различных хозяев. Коронавирус встречается у многих млекопитающих, рептилий, рыб. Все изменения в структуре вируса направлены на освоение им новых биологических ниш, это адаптация к организму хозяина, способность избежать воздействия иммунитета.Тем не менее буквально на днях появились обнадеживающие новости: ученые Института иммунологии в Ла-Хойя впервые обнаружили сильный иммунный ответ против вируса SARS-CoV-2 среди переболевших COVID-19. Результаты исследования продемонстрировали, что иммунитет способен разными способами распознавать новый коронавирус, и развеяли опасения, что усилия по разработке эффективной вакцины могут оказаться бесполезными. Об этом сообщается в пресс-релизе на MedicalXpress.
По данным на начало мая, в фазу клинических испытаний вступили по всему миру 8 вакцин от коронавируса: две в США, четыре в Китае, одна в Великобритании и одна в Германии. Ожидается, что в течение этого года в ФРГ добавятся, скорее всего, еще три.
В Америке на днях заявили об успешном испытании на людях вакцины от COVID-19. Препарат тестировали компания Moderna и специалисты Национальных институтов здравоохранения США, сообщает ТАСС. Участников клинических испытаний разделили на несколько групп, которые получали разные дозы вакцины. У тех, кто получал наименьшую дозу, антитела выработались примерно в том же количестве, которое наблюдается у людей, переболевших коронавирусной инфекцией. При этом у тех, кто получал большую дозу, антител в организме к окончанию испытаний было выявлено намного больше, чем у пациентов с коронавирусом после излечения. «Команда Moderna в ускоренном темпе работает над тем, чтобы приступить в июле к третьему этапу испытаний вакцины и в случае его успеха подать заявку на лицензирование препарата», — указал глава компании Стефан Бансель.
Над решением задачи производства вакцины от нового коронавируса работают также семь российских научных учреждений. В СМИ называются, в частности, научный центр «Вектор» Роспотребнадзора в Новосибирске, который уже выпускает тест на коронавирус и сейчас разрабатывает шесть вариантов вакцины, петербургская биотехнологическая компания Biocad (два или три варианта), НИИ вакцин и сывороток в Санкт-Петербурге, Федеральное медико-биологическое агентство (ФМБА) и Российская академия наук (РАН) в Москве.
Всего же в разных частях планеты насчитывается порядка 100 проектов по созданию вакцины от COVID-19. К примеру, французская компания Sanofi разрабатывает ее совместно с британской GlaxoSmithKline, китайская Sinopharm Group — вместе с Уханьским институтом вирусологии, американский гигант Pfizer — совместно с небольшой немецкой BioNTech, первой в Германии получившей разрешение на клинические испытания своей разработки, пишет dw.com.
Так ждать ли нам уже в этом году самую актуальную на сегодня прививку? Несмотря на бравурные заявления в СМИ, ответить, что называется, под присягой на этот вопрос не берутся ни политики, ни медики. По прогнозам Всемирной организации здравоохранения, только на разработку иммунобиологического препарата может уйти от 15 до 18 месяцев. Кроме того, масса вакцин-кандидатов, прошедших первую и вторую фазы клинических исследований, на завершающей третьей ввиду отсутствия эффективности объявляются непригодными.
Годы исследований и миллиарды у.е.
Прежде чем попытаться понять, можно ли создать вакцину и запустить ее в производство в течение года, давайте определимся, что представляет собой вирус и почему одна из его разновидностей буквально парализовала планету в век высоких технологий.

— Что представляет собой создание нового препарата?
— Разработка вакцины — многоэтапный и длительный по времени процесс, который начинается с идентификации возбудителя заболевания, изучения его свойств. У возбудителя инфекционного заболевания есть факторы патогенности (антигены), которые запускают патологический процесс, поэтому важно установить, на какие именно антигены иммунная система вырабатывает защитные антитела.
Следующий этап — выбор технологии производства препарата. Здесь разработчики определяются с тем, какой именно тип вакцины лучше подойдет для эффективной профилактики заболевания: живая аттенуированная, инактивированная (с убитым цельным вирусом или бактерией), субъединичная (с очищенным антигеном), рекомбинантная и т. д. На данном этапе составляется рецептура вакцины — количественное и качественное описание химических компонентов, входящих в конечный продукт (антигены, адъюванты, стабилизаторы, консерванты, электролиты и др.). После определения рецептуры готовят кандидатный вакцинный препарат, который проходит этапы доклинических и клинических исследований.
Доклинические исследования проводят вне живого организма (клетки, ткани), а также на животных (мыши, крысы, хомяки, хорьки, приматы), для этого подбирается необходимая чувствительная биологическая модель.
Клинические исследования проводятся на людях и состоят из трех фаз. В первой вакцина-кандитат тестируется на небольшом количестве участников (как правило, десятки человек), это добровольцы и только взрослые (детям в 1-й фазе участвовать запрещено). После того как будут получены убедительные данные о безопасности и иммуногенности вакцины, приступают ко второй фазе клинических исследований — набирается целевая группа (уже сотни человек). В этой фазе в числе прочего подбирают дозы, схемы введения препарата. Дети во вторую фазу исследования включаются только с письменного согласия родителей.
В третьей фазе клинических исследований проводят оценку эффективности вакцины среди различных возрастных групп с увеличением выборки 1000 человек и более. Для того чтобы оценить эффективность вакцинации, необходимо организовать проспективное исследование с позиций доказательной медицины, где есть подбор контрольной группы к опытной. В последующем проводится оценка эффективности исходя из количества заболевших в обеих группах. Также ведется учет побочных реакций.

— Длительность таких исследований обычно составляет 1—2 года и более в зависимости от вакцины. Производство вакцин — это также сложный многоступенчатый и длительный процесс, на который в среднем тратится от 4 месяцев до 3 лет, и следует сказать, что основная часть этого времени (примерно до 70%) уходит на контроль качества. На начальных этапах в лаборатории готовится биологический посевной материал (вирусы, бактерии), далее следует накопление этого материала (культивирование в клетках, выращивание на питательных средах). Затем проводят выделение вирусной или бактериальной массы, ее очистку от балластных примесей (остатки среды культивирования). А дальше этапы зависят от того, какой тип препарата требуется произвести. На заключительной фазе приготовления вакцины проводят очистку препарата, концентрирование, сушку при необходимости, расфасовку и упаковку.
— Какова примерная стоимость разработки и производства вакцины?
— Разработка вакцины с нуля — это миллиарды долларов и годы исследований до выхода на рынок. По оценкам фонда CEPI (Коалиция по инновациям в области обеспечения готовности к эпидемиям), который инвестирует в производство вакцин в период вспышек эпидемии, пандемии, для разработки вакцин-кандидатов и запуска их в производство требуется минимум 2 миллиарда долларов. Налаженное производство вакцин — это миллионы долларов. Ведущие позиции на мировом рынке вакцин занимают компании GlaxoSmithKline, Sanofi, Pfizer, Merck, Novartis AG, Baxter International. Крупнейшим рынком вакцин являются США, страны Европы (Бельгия, Франция, Германия, Нидерланды). Довольно быстрыми темпами развивается индийское и китайское производство вакцин. Более чем в 70 стран поставляет вакцины Бразилия. Крупнейшими российскими производителями иммунобиологических препаратов являются фармацевтические компании «Микроген», «Петровакс Фарм».
— А у Беларуси есть шанс наладить свой выпуск?
— С одной стороны, у нас нет условий, которые препятствовали бы развитию импортозамещения в этой сфере. Конечно, производство вакцин требует инновационных технологий и относится к числу высокотехнологичных и дорогостоящих. С другой стороны, несмотря на всю привлекательность для инвесторов, существуют и серьезные экономические риски, которые обусловлены сложными технологическими процессами, дорогостоящим оборудованием, высококвалифицированным персоналом, процедурой сертификации производства, лицензирования и регистрации вакцин. Для таких проектов требуется поддержка государства.
Можно пойти по более рентабельному и экономически выгодному пути: например, задействовать трансфер технологий, розлив иностранных компонентов, приобретение вакцин в форме In bulk (ампулы, растворы) с последующей фасовкой. Не исключено, что в перспективе это направление будет представлено и у нас. Это вопрос времени и, главное, потребности. В Беларуси вакцинация в рамках Национального календаря профилактических прививок полностью финансируется государством, и необходимо отметить, что, согласно календарю, населению осуществляется плановая иммунизация против 12 инфекций.
Укол разума

— Внутреннее потребление должно быть поддержано высокой внутренней потребностью. Учитывая эпидемический процесс вакциноуправляемых инфекций в Беларуси, отсутствие особенной эндемичности для территории нашей страны и численность целевых групп, создание системы производства вакцин с нуля может быть более затратным, чем налаженный импорт.
Если приоритетной целью производства определить экспорт, в данном случае необходимо предусмотреть возможности в отношении конкурентоспособности. Производство может быть оправдано в случае уникальности препарата, если рынок в данном сегменте не насыщен либо технология является новой. Рентабельность производства может быть выше в случае массовости экспорта. Для уникальных препаратов необходима разработка технологий, научная, нормативная, экспериментальная база, для массовости производства — производственная база, наличие целевого заказчика. Таким образом, начальным этапом в развитии нового для страны направления может быть научная разработка уникальных технологий для дальнейшей их реализации производителям, производство сырья и полуфабрикатов на базе уже имеющихся предприятий для поставки на заводы — изготовители вакцин.
Немаловажным этапом на этом пути является также усиление системы биобезопасности страны, создание законодательной базы в отношении биологической защиты с целью дальнейшего развития перспективы работы лабораторий с вакцинными штаммами.
— Национальным собранием нашего созыва принят во 2-м чтении Закон о лекарственных средствах, которым предусмотрены процедуры ускоренной регистрации, а также раннего доступа к лекарственным средствам, — говорит Владимир Гацко. — Таким образом, создана законодательная основа для максимально раннего применения вакцины. Также ежегодно принимается Закон о бюджете, в котором есть раздел, посвященный вопросам здравоохранения. Мы можем регулировать и дополнительное выделение финансирования на закупку необходимых лекарственных средств для лечения пациентов и необходимых профилактических прививок.
Объединить усилия
Председатель Коллегии Евразийской экономической комиссии Михаил Мясникович считает перспективным сотрудничество стран Евразийского экономического союза в фармацевтической сфере, в том числе по совместному созданию вакцины от COVID-19. Такое мнение он высказал, отвечая на вопросы во время международного форума «Содействуя евразийской экономической интеграции: фактор делового сотрудничества», который состоялся в режиме видеоконференции, пишет БЕЛТА.— Насколько я информирован, сейчас стороны консультируются по многим вопросам и имеют хорошие заделы ученых и практиков, — сказал Михаил Мясникович. — Я еще раз проработаю этот вопрос, какие конкретно учреждения участвуют в совместных программах. У нас был подход по первой биотехнологической программе, думаю, мы вернемся к этой теме.
Председатель Коллегии ЕЭК обратил внимание на недостаточность обеспечения рынка ЕАЭС лекарствами собственного производства:
— Сегодня у нас вообще очень бедный рынок лекарств в целом. И Россия, и Беларусь, и Казахстан закупают в огромных объемах как фармацевтические субстанции, так и готовые лекарственные средства для нужд собственного рынка — для стационаров и непосредственно населения. Безусловно, надо выходить на очень мощную программу, возможно, даже с участием компаний из третьих стран по производству лекарств и соответствующих фармсубстанций.
В ТЕМУ
Предотвратить инфекционный апокалипсис
В январе 1897 года человеку впервые была введена вакцина от чумы, разработанная учеником Л. Пастера русским ученым Владимиром Хавкиным. Именно благодаря этим прививкам удалось остановить пандемию, которая с VI по XIX век буквально выкосила 50% населения Европы.

Первую прививку от натуральной оспы сделал в конце XVIII века английский врач Э. Дженнер, положив тем самым начало будущей ликвидации этого страшного заболевания, последний случай которого был зарегистрирован в октябре 1977 года в Сомали.
В начале XX века французские ученые Альбер Кальметт и Камиль Герен создали первую человеческую вакцину на основе штамма ослабленной живой коровьей туберкулезной бациллы — вакцину БЦЖ (BCG — Bacille Calmette-Guerin).
Начало масштабного использования полиомиелитной вакцины привело к резкому сокращению заболеваемости (в первой половине прошлого века полиомиелит поражал десятки тысяч людей ежегодно). В Беларуси в довакцинальном периоде ежегодно около 1 тысячи детей заболевало полиомиелитом, и значительная часть из них оставалась инвалидами, более 50 тысяч малышей заражались корью и краснухой, около 33 тысяч — эпидемическим паротитом и более 11 тысяч человек заболевало дифтерией.
В новейшей истории причиной эпидемий и пандемий остается вирус гриппа. «Испанка», бушевавшая в 1918—1919 годах, унесла жизни 50—100 миллионов человек. Азиатский грипп в 1957-м похоронил порядка 2 миллионов человек. Гонконгский грипп в 1968 году — около 34 тысяч человек.
По оценкам ВОЗ, ежегодные эпидемии гриппа приводят к 3—5 миллионам случаев тяжелой болезни и к 290 000—650 000 случаев смерти от респираторных заболеваний.
konopelko@sb.by
Ближайшее будущее человечества, несмотря на развитие систем здравоохранения, появление новейших средств и способов диагностики, лечения и профилактики, будет сопряжено с инфекционными болезнями. Их распространению уже сейчас способствуют вооруженные конфликты, экономические кризисы, глобальные миграционные процессы, изменение климата.
pixabay.com
Рисунок Олега Попова